Tradicionalmente la lixiviación de los minerales oxidados de cobre consiste en disolver los iones de cobre apilando la mena chancada y aglomerada para su posterior irrigación con soluciones ácidas, sin tener mayores problemas de reacción química, obteniendo de esta manera un PLS, solución rica en cobre que continúa a las etapas posteriores de concentración y purificación: extracción por solventes (SX) y electro-obtención (EW).
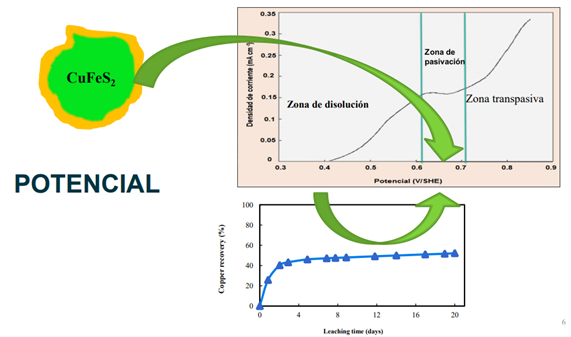
Realizar lo mismo con minerales sulfurados no resulta tan simple, debido a que la solución PLS obtenida es muy diluida en iones cobre debido a que los minerales sulfurados de cobre tienen una cinética lenta de disolución. Como ejemplo, la calcopirita (CuFeS2) el cual es el mineral de cobre más abundante en la corteza terrestre, pero además es el más refractario a la lixiviación. Al intentar lixiviarla se produce al inicio una pequeña disolución, sin embargo, al pasar un corto periodo de tiempo se detiene, producto de la formación de una capa pasivante en la superficie de la partícula, cuya naturaleza aun es controversial diciéndose que es una capa de azufre elemental, capa de óxido de hierro, capa porosa de azufre, capa de un sulfuro menos reactivo que la cpy, capa de metal deficiente de un polisulfuro de cobre entre otras. Esta capa inhibiría subsecuentes disoluciones. Se debe hacer notar que las reacciones que ocurren al tratar de disolver a los minerales sulfurados son reacciones electroquímicas que no sólo dependen de pH para que ocurran, sino que también del potencial redox. Investigaciones han tratado de maximizar la disolución de estos minerales notando que esta es muy dependiente del potencial como lo indica la figura donde bajo esas condiciones de 0.2 M de HCl y 0.5 g/L de cúpricos agregados a la solución lixiviante se logra maximizar la disolución (mostrado como densidad de corriente que es directamente proporcional a la cantidad de cobre disuelto) dentro de un rango de potencial. La figura muestra tres zonas la primera donde se logra maximizar la disolución (zona de disolución), la zona de pasivación donde se detiene la disolución y por último la zona transpasiva donde a potenciales altos la calcopirita logra disolverse nuevamente en condiciones altamente oxidantes.
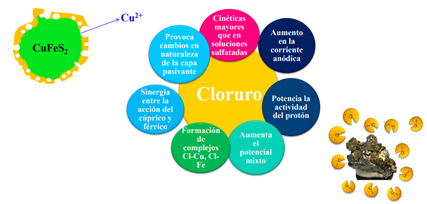
Ventajas de la lixiviacion clorurada
Los minerales sulfurados de cobre que mejor se lixivian son en orden: calcosina (Cu2S), covelina (CuS), bornita (Cu5FeSO4), calcopirita (CuFeS2) y finalmente la enargita (Cu3As4).
Se ha observado que los parámetros que afectan la disolución de la calcopirita son:
- Aglomeración, al agregar iones cloruro, mejora la disolución
- Concentración de Cu2+ y Cl-
- Acidez
- Oxígeno disuelto
- Sinergia de iones Fe/Cu
- Potencial redox
- Regadío, se requieren tiempos de reposo para reactivar la lixiviación (riego on/off)
- Curado, mayor tiempo de curado, aumenta la extracción de cobre
- Tamaño de partícula
Para continuar estudiando la lixiviación clorurada se pueden tener en consideración los siguientes tópicos a futuro:
- Cómo trabajar a altas concentraciones de iones cloruro sin causar problemas en la operación.
- Cómo utilizar las bondades de los medios clorurados y al mismo tiempo evitar que cualquier tipo de capa sea formada en la superficie del mineral y así aumentar aún más la cinética de disolución de la calcopirita.
- Poner más atención a las etapas previas a la lixiviación. Establecer metodologías específicas de aglomerado y curado para el éxito de estas etapas anteriores a la lixiviación.
- Sistema de regadío eficiente para enfrentar el uso de grandes cantidades de iones cloruros en el refino.
- Calentar la pila, ¿por qué no?
- Lixiviar nuestros concentrados, ¿por qué no?
- Modificación de las etapas de extracción por solventes, cambiando diseño, dosificaciones de extractantes e incluir etapas de lavado.
Extracto de presentación en Webinar IMetChile “Lixiviación de Minerales de Cobre con Sales de Cloruro”, mayo 2020.
Autora: Dra. Lilian Velásquez Yévenes, Universidad de Talca.